一、丙肝治疗的现状
丙肝即丙型肝炎(Hepatitis C),根据 WHO 数据,全球有 1.3 亿-1.5 亿慢性丙肝患者,而中华医学会《丙型肝炎防治指南( 2015 年更新版)》数据:2006 年全国血清流行病学调查显示,我国 1~59 岁人群 HCV 流行率为 0.43%,加上高危地区,约有 1000 万患者。急性丙肝病毒感染者中,55%~85%会转变成慢性肝炎,慢性丙肝 20 年的肝硬化发生率为 5%~15%,其中的 2%~4%会转变成肝癌。目前 WHO 推荐的治疗方案有三种,即利巴韦林+PEG 修饰干扰素α,利巴韦林+PEG 修饰干扰素α+特拉匹韦/波曲普韦和索非布韦+利巴韦林(+ PEG 修饰干扰素)。因为不同丙肝药物在不同国家的上市进度不一样,所以各国主推疗法也不一样,美国推荐的疗法主要是以Harvoni,Sovaldi,Viekira park 为基础iii,英国则以 Sovaldi,OLYSIO 为基础,而我国无新型抗丙肝药物上市,主推疗法仍是利巴韦林+PEG 修饰干扰素α,不过2015年更新的临床指南,加入了索非布韦、达卡拉韦等直接抗病毒药物(DAA)。

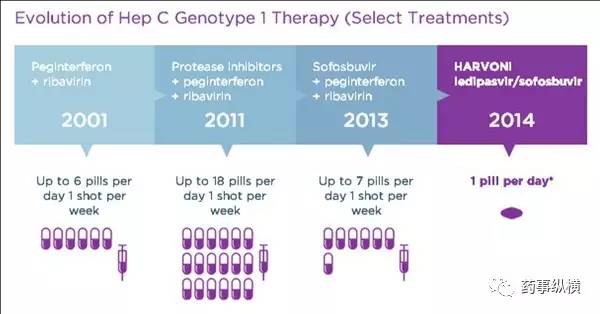
近年来丙肝治疗已经取得突破性进展,Harvoni 官网上的图片很好地解释了近 15 年的丙肝疗法变化。丙肝治疗的突破性进展并不只限于剂量的减少,更关键的是 SVR(Sustained virologic response)的大幅提高和治疗周期的大幅减少。利巴韦林+PEG 修饰干扰素α需要连续治疗 48-72 周,根据文献报道,利巴韦林+PEG 修饰干扰素α治疗 48 周,停药后的 12 周 SVR 只有 44%-47%v,而最新的鸡尾酒疗法(Harvoni,Viekira park,Zepatier)只需治疗 12-24 周,SVR 达90%以上,部分基因类型则接近 100%。正因为丙肝治疗的突破性进展,全球丙肝市场才得以爆发。2015 年,全球丙肝市场已达 240 亿美元,大约是 2010 年的 9 倍。不仅如此,根据 IMS 数据,2020 年丙肝市场将达 360 亿美元,其中新兴市场为 60 亿美元。

[url=]吉利德[/url]
吉利德凭借Sofosbuvir的优势独霸丙肝市场,Sofosbuvir 是第一个上市的 NS5B RNA 聚合酶抑制剂,2013 年 12 月 6 日获 FDA 批准用于基因 1-4 型丙肝,如今在 ICH 国家范围内均已获批。Sofosbuvir 是第一个可以无需干扰素治疗丙肝的药物,并且将治疗周期缩短至 12-24 周,SVR 提高至 80%以上。正因如此, Sofosbuvir 引爆了全球丙肝治疗市场,2014 年 Sofosbuvir 的销售额超过 100 亿美元,紧接着吉里德以 Sofosbuvir 为基础上市了第一个丙肝鸡尾酒 Harvoni,进一步提高了 Sofosbuvir 的疗效,而且适应症也拓宽至基因 1-6 型丙肝。2015 年吉里德凭借 Harvoni 和 Sovaldi 拿下了 80%的丙肝市场,两个药的销售额达 191.4 亿美元。在Harvoni的基础上,吉利德又开发了Epclusa,该产品是由sofosbuvir(400mg)和velpatasvir(100mg)组成的泛基因型丙肝鸡尾酒疗法,可用于全部6种基因型丙肝患者的治疗。其中,sofosbuvir是一种NS5B核苷类似物聚合酶抑制剂,velpatasvir则是一种泛基因型NS5A抑制剂,上市一周销售额达6400万美元。然而,吉利德
对丙肝产品的升级并未停止,8周一疗程的三联鸡尾酒Sofosbuvir/ Velpatasvir/ Voxilaprevir已经申报FDA。
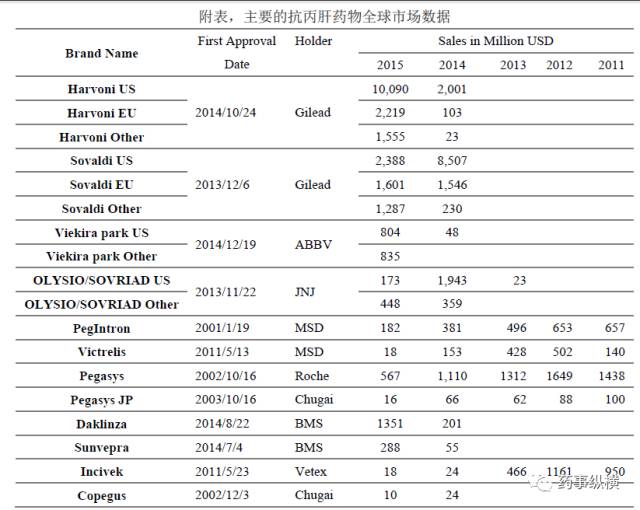
艾伯维 Dasabuvir 是第二个 NS5B 抑制剂,与吉里德策略不同的是,艾伯维直接将 Dasabuvir 做成鸡尾酒上市,2014 年 12 月 19 日获 FDA 批准用于基因 1,4 型丙肝治疗,商品名为 Viekira park。Viekira park 的疗效和 Harvoni 差不多,但存在用药不方便,而且去年 FDA 提出警告,称 Viekira Pak和 Technivie 可能会增加严重肝损伤的风险,尤其是对于那些患有晚期肝病的患者,这样一来,Viekira park 的竞争力和市场空间大打折扣。不过艾伯维对Viekira进行了升级,做成Viekira XL,将给药频率降低到每日一次,而且最新的丙肝鸡尾酒Glecaprevir/ pibrentasvir 也已经在注册的路上,能否搬回一局就看2017年。
默沙东默沙东是第一个做丙肝DAA的公司,拥有最多的专利,但Boceprevir疗效不给力,没有占到先机。其第一个鸡尾酒,即 Zepatier,2016年才上市,Zepatier由Elbasvir 和Grazoprevir组成,其中Elbasvir是一个 NS5A 抑制剂,与 Grazoprevir 是一个NS4/3蛋白酶抑制剂。Zepatier 于 2016 年 1 月 28 日获 FDA 批准用于基因 1,4 型丙肝治疗,根据近期的临床数据,Zepatier 的疗效不亚于 Harvoni 和 Viekira park。该产品的优势是可以用于肾损伤患者,而且定价便宜。目前尚没有 Zepatier 的整年市场数据,汤森路透分析师预测,Zepatier 在 2020 年的销售额将达 15 亿美元vii。
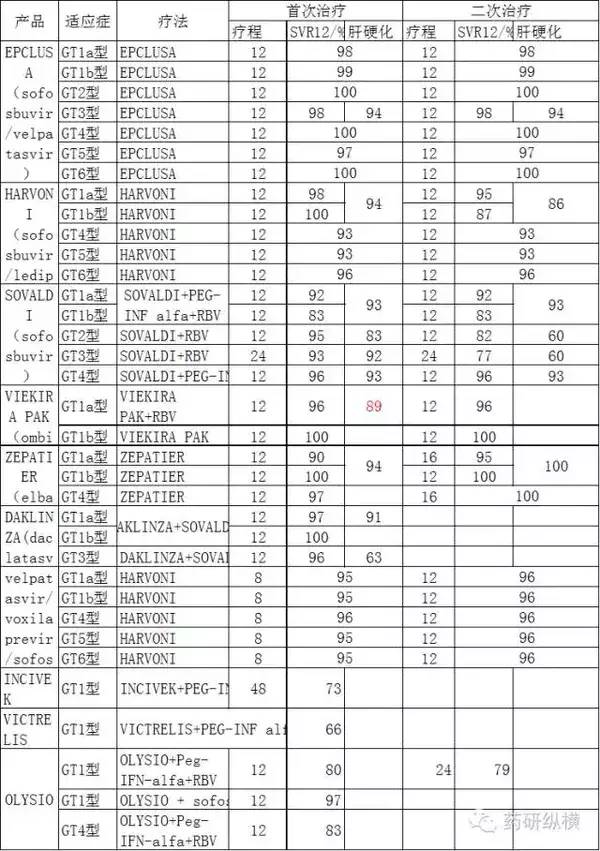
丙肝DAA疗效对比(数据来自FDA说明书)
百时美施贵宝 Daclatasvir 是 BMS 开发的 NS5A 抑制剂,联合 Sofosbuvir 用于基因 3 型丙肝治疗。2015 年 Daclatasvir 的销售额为 13.5 亿美元,Daclatasvir 和 Asunaprevir 使 BMS 占得丙肝市场 7%的份额。此外,BMS也开发了新一代丙肝鸡尾酒Asunaprevir/ beclabuvir/ daclatasvir,近期将提交申报资料。
Other 其它产品主要是 NS4/3 蛋白酶抑制剂和干扰素α,其中 NS4/3 蛋白酶抑制剂包括Boceprevir,Vaniprevir,Telaprevir 和 Simeprevir。这几个产品中,除 Simeprevir 仍被美国推荐联合 Sofosbuvir 用于治疗基因 1 型丙肝外,其它几个产品已经在美国市场的激烈竞争中濒临淘汰。2015 年 Simeprevir 的销售额为 6 亿美元,较 2014 年的 23 亿美元,降幅达 73%。干扰素方面,自 Sofosbuvir 上市以来,干扰素α市场份额一直下滑,销售额从 2010 年 28 亿美元将至 2015 年的 8 亿美元。
二、丙肝药物的研发情况
从汤森路透和Springer adisinsight来看,丙肝药物的研发尚未变冷,大量产品还处在临床前阶段。处于三期和在申报阶段的产品并不多,说明未来五年还有大量产品上市,详情见下表:
在研丙肝药物pipeline的进展情况

从靶点来看,新产品中NS5B较多,其次是NS5A和NS4/3,也许是收到索非布韦的启发,Thomson和Adisinsight数据库中不同靶点在研药物如下表所示。
在研丙肝药物pipeline的靶点分类

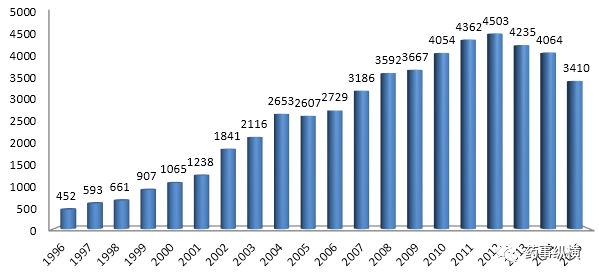
从专利申请来看,丙肝新产品的专利申请高峰为2012年,这也侧面反映很多丙肝新药还在临床前阶段。2013年开始,丙肝药物的专利申请开始下滑,说明新分子、新靶点的开发逐渐减少,大量产品开始从发现阶段向临床阶段转移。
丙肝药物的专利申请情况
三、丙肝药物研发的未来
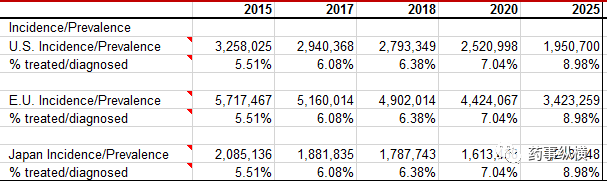
根据datamonitor数据库的丙肝流行病率数据预测,2020年欧美日丙肝患者将减少20%,2025年将减少一半。随着患者的大量治愈,加之各种鸡尾酒的大量出现,丙肝的治疗费用会大幅下降,市场也必将慢慢下滑。
2015-2025丙肝流行病学数据
从现有的产品销售数据来看,很多丙肝DAA的光鲜都是昙花一现,如特拉匹韦,2016年Harvoni的销售额也不会再像2015年那么光鲜。最主要的原因在于丙肝产品更新换代太快,产品没有最好,只有更好,没有最便宜,只有更便宜,这是丙肝治疗市场和研发的必然趋势。
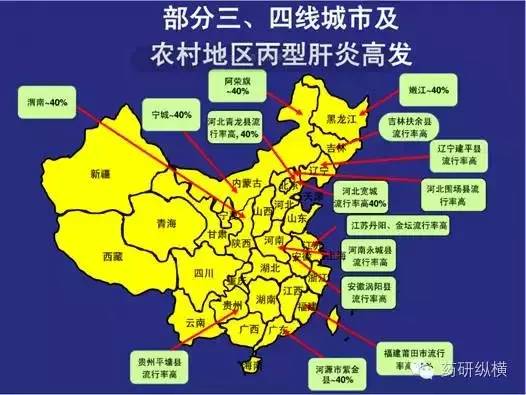
三、丙肝药物的中国化
中国拥有1000万左右的丙肝患者,但尚无一个丙肝DAA上市,尽管很多产品已经获得CFDA的优先审评,但上市时间也要推迟到2018年以后。因为中国有1000万的患者,中国将是欧美日以外制药巨头们必争的市场。因为大量重磅级进口鸡尾酒已经在申报的路上,国内的DAA研发企业很难分到大蛋糕。因此,笔者觉得与其做新的DAA开发,还不如做仿制。一则新药研发成本太高,二则,竞争太激烈,疗效一般的产品还未上市就要被淘汰,三则丙肝DAA更新太快,研发管线薄弱的公司很容易昙花一现。仿制方面,索菲布韦2024年到期,可以作为一个仿制的主要目标。
高昂的治疗费用,如没有国家医保的支持,这些产品在中国很难卖起来。而根据以往的经验,原研产品在专利期内进医保的可能性不大。如果Harvoni一类的产品进中国医保,必然大量患者都会去治疗,医保根本抗不住。因此这些产品要进医保,除非大幅降价或者等专利到期,仿制药上市。在此,笔者敢大胆推测,短期内中国的丙肝市场“火”不起来,也不会有大量的患者被治愈。康安途的印度仿制药依然是我国饼干患者的首选治疗方案。
| 欢迎光临 海外就医|丙肝|肿瘤|试管婴儿 - 康安途海外医疗论坛 (http://bbs.kangantu.org/) | Powered by Discuz! X3.2 |